Инсулиннің гендік инженериясы
Инсулин - ұйқы безінің гормонын | реттейтін | көмірсулар алмасуы және каддтың қалыпты деңгейін сақтаупақанда. Денедегі бұл гормонның жетіспеушілігі өте ауыр аурулардың бірі - өлім себебі ретінде жүрек-тамыр аурулары мен қатерлі ісік ауруынан кейін үшінші орында тұрған қант диабеті. Инсулин - бұл кішкене глобула | құрамында 51 аминқышқылының қалдықтары бар және екі дисульфидті көпірмен байланысқан екі полипептидті тізбектен тұратын ақуыз. Құрамында бір тізбекті ұрықтың прекурсорсулин, синтезделеді Қой мақсатты сигнал пептиді (23 амин қышқылы қалдықтары) және 35 байланыстырушы пептид (C-пептид). Сигналдық пептид алынып тасталғаннан кейін А және В инсулин тізбектері қосылған жасушада 86 аминқышқылының қалдықтарынан проинсулин түзіледіС-нейтвид, бұл оларға дисульфидті байланыс үшін $ 3 бағдар береді. С пептидінің протеолитикалық бөлінуінен кейін инсулин түзіледі.
Қант диабетінің бірнеше түрлері белгілі. Емделу үшін пациентке инсулин қажет (аурудың инсулинге тәуелді түрі), бұл гормонды синтездейтін жасушалардың (ұйқы безіндегі Лангерган аралдары жасушалары) іріктелген өлімінен туындайды. Инсулинмен емдеуді қажет етпейтін қант диабетінің түрі жиі кездеседі, оны тиісті диеталар көмегімен басқаруға болады және қайтадан: Әдетте, ірі қара мал мен сиырдың ұйқы безі ет және консервілеу өндірісінде қолданылмайды және гормон өндірілетін фармацевтикалық компанияларға арналған тоңазытылған вагондарға орналастырылады. 100 г кр алу үшін! Таллик инсулиніне 800-1000 кг шикізат қажет
Екі тізбектің синтезі және олардың инсулин алу үшін дефицидті байланыстармен байланысы 1963 және 1965 жж. Жүргізілді. АҚШ, Қытай және Германиядағы үш зерттеу тобы. 1980 жылы Данияның «Ново Индустри» компаниясы В тізбегіндегі аланиннің 30-шы қалдықтарын треониндік қалдыққа ауыстыру арқылы шошқа инсулинін адам инсулиніне айналдыру әдісін ойлап тапты. Екі инсулин де белсенділігі мен әрекет ету ұзақтығында ерекшеленбеді.
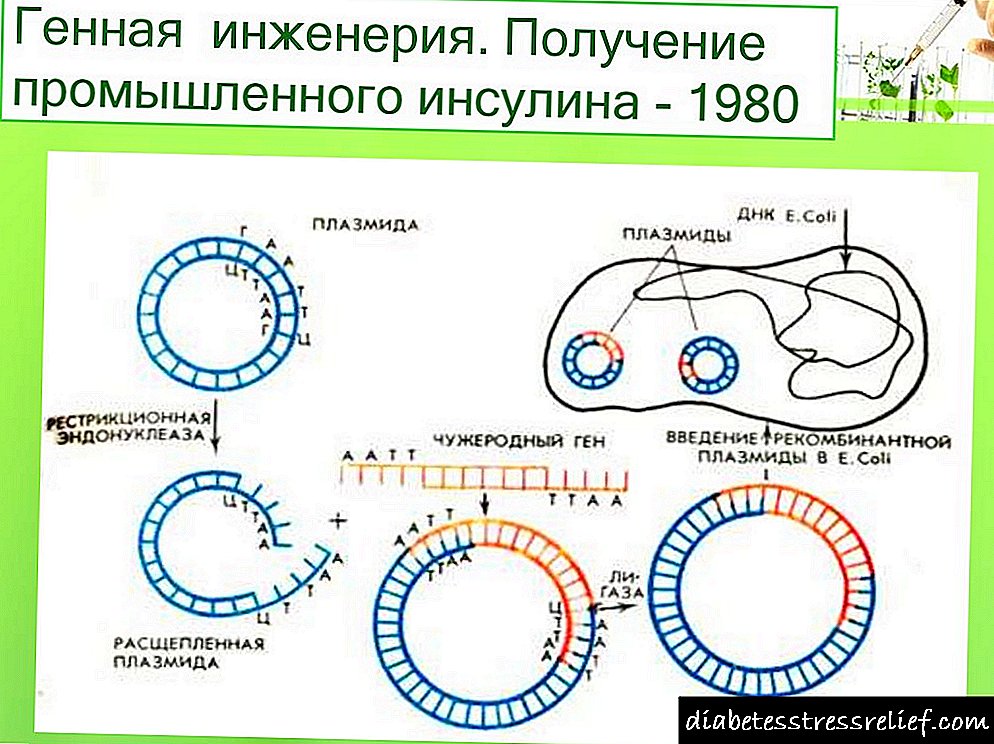
Инсулиннің гендік инженериясымен жұмыс шамамен 20 жыл бұрын басталды. 1978 жылы егеуқұйрық проинсулинін шығаратын Escherichia coli штаммының өндірісі туралы хабарлама пайда болды (АҚШ). Сол жылы адамның жеке инсулин тізбегі жасушаларда олардың синтетикалық гендерін көрсету арқылы синтезделді.Е.коли(5.11-сурет). Синтезделген гендердің әрқайсысы фермент генінің 3-аяғына бейімделді (3-галактозидаза және векторлық плазмидаға енгізілді)(pBR322).ЖасушаларЕ.колиосындай рекомбинантты плазмидтермен қайта құрылып, метионин қалдықымен қосылған p-галактозидазаның фрагменттерінен және А немесе В инсулин пептидінен тұратын гибридті (химиялық) ақуыздар шығарылды. Химиялық ақуызды цианоген бромидімен өңдеген кезде пептид шығады. Алайда, қалыптасқан инсулин тізбектері арасындағы дисульфидті көпірлерді жабу қиынға соқты.
1981 жылы про-инсулин аналогы, мини-С-про-инсулин синтезделді, оның барысында 35-бірлік С-пептид алты аминқышқылдарының сегментімен ауыстырылды: arg-arg-gly-ser-lys-arg және оның өрнегі көрсетілгенЕ.коли.
1980 жылы В.Гилберт және оның әріптестері инсулинді мРНҚ-ны егеуқұйрықтегі Р-жасушалық ісіктен бөліп алып, кері транскриптазаны қолдана отырып, одан cDNA алды. Алынған cDNA плазмидаға енгізілдіpBR322Е.колипенициллиназа генінің ортаңғы бөлігінде. Рекомбинантты плазмида проинсулиннің құрылымы туралы ақпарат болды.МРНҚ-ны аудару нәтижесінде пенициллиназа мен проинсулин тізбегі бар жасушаларда гибридті ақуыз синтезделді, олар осындай ақуыздан трипсинмен сіңірілді.
1978 жылы Акаданың жетекшілігімен Биоорганикалық химия институтының қызметкерлері. Овчинников Ю.А., нейропептидтер синтезін кодтайтын екі құрылымды гендер синтезделді:лейцин-энкефалин және брадикинин.Синтезделген лейциндік энкефалин генінің екі «жабысқақ» ұшы бар:
Алынған синтетикалық ген прототип және E. coli P-galactosidase ақуыз генінің проксималды бөлігі бар табиғи ДНҚ фрагментімен бірге енгізілдіЕ.колиплазмидаға
Инсулин алу, гендік инженерия әдістері, биотехнология - курстық жұмыс

1. Инсулиннің құрылымы мен функциялары 5
1.1. 5 инсулин молекуласының құрылымы
1.2. Инсулиннің биологиялық маңызы 7
1.3. Инсулин биосинтезі 8
2. Инсулиннің генетикалық инженериясы 10
2.1. Дәрілерді синтездеу үшін гендік инженерлік әдістерді қолдану 10
2.2. Генетикалық инженерия әдістері 11
2.3. Инсулиннің гендік инженериясы 14
Мәтіннен үзінді
Сонымен қатар, екі компонент бір уақытта гибридті ақуыздың құрамында болуы мүмкін. Сонымен қатар, гибридті ақуыздарды құру кезінде көп өлшемділік принципін қолдануға болады - гибридті ақуызда мақсатты полипептидтің бірнеше көшірмесінің болуы, ол мақсатты өнімнің шығымдылығын едәуір арттыра алады.
Ұлыбританияда адам инсулинінің екеуі де биологиялық белсенді гормонның молекуласына қосылған E. coli көмегімен синтезделді. Бір клеткалы ағза өзінің рибосомаларына инсулин молекулаларын синтездеуі үшін оны қажетті бағдарламамен қамтамасыз ету керек, яғни оған гормондық генді енгізу керек.
Рекомбинантты инсулин Ресей ғылым академиясында Э.Коли гендік-инженерлік штаммдарын қолдану арқылы алынды. Гибридті прекурсорлы ақуыз өсіп келе жатқан биомассадан, мөлшерде көрінеді
40. Преопринсулині бар жасушалық ақуыздың жалпы саны.
Оның in vitro инсулинге ауысуы in vivo тәрізді ретпен жүреді - жетекші полипептид бөлініп, препросулин тотығатын сульфитолиз сатысы арқылы инсулинге айналады, содан кейін үш дисульфидті байланыстың редуктивті жабылуы және байланыстырушы С-пептидтің ферментативті оқшаулануы жүреді. Ион алмасу, гель және HPLC хроматографиялық тазартулар сериясынан кейін жоғары тазалық пен табиғи белсенділікке ие инсулин алынады.
Инсулинді алу үшін 8, 9, 10 метиониннің қалдықтары арқылы N-терминалына қосылған сызықтық проинсулин мен стафилококк ауруының ақуызынан тұратын гибридті ақуызды білдіретін плазмидаға енгізілген нуклеотидтер тізбегі қолданылады.
Рекомбинантты штамм жасушаларының қаныққан биомассасын өсіру оқшаулау және дәйекті түрде өзгеруі инсулинге әкелетін гибридті ақуызды өндіруді бастайды.
Басқа жолмен де мүмкін: адамның проинсулині мен полихистидиннің құйрығынан тұратын рекомбинантты ақуызды бактериалдық жүйеде метионин қалдықымен алу. Ни-агароза мен бромды бөліп алу арқылы колоннадағы хелат хроматографиясын қолдану арқылы оқшауланған.
Оқшауланған ақуыз S-сульфатталған. Анион алмасу шайыры мен RP (кері фаза) жоғары өнімді сұйықтық хроматографиясында ион алмасу хроматографиясымен тазартылған алынған проинсулинді картаға түсіру және масс-спектрометриялық талдау адамның туған проинсулинінің дисульфидті көпірлеріне сәйкес келетін дисульфидті көпірлердің болуын көрсетеді.
Жақында генетикалық инженерия көмегімен рекомбинантты инсулинді алу процедурасын жеңілдетуге көп көңіл бөлінді.Мәселен, интерлейкин көшбасшы пептидінің лизин қалдықтары арқылы N-терминалына қосылған проинсулиннен тұратын ақуыз алуға болады
2. Белок тиімді әсер етеді және инклюзивті денелерде локализацияланған. Оқшауланғаннан кейін инсулин мен С-пептид өндіретін ақуыз 5, 8, 10 трипсинмен жабылады.
Алынған инсулин мен С-пептид RP-HPLC арқылы тазартылады. Ерітілген құрылымдарды құру кезінде тасымалдаушы ақуыз мен мақсатты полипептид массаларының арақатынасы өте маңызды.
Sfi I шектеу алаңын өткізетін амин қышқылы кеңейткіштерінің көмегімен С-пептидтер және протеин трипсинін кейінгі ас қорытуға арналған тіректің басында және соңында екі аргинин қалдықтары бастың құйрығы қағидасына сәйкес қосылады.
Бөлінетін өнімдердің HPLC көрсеткендей, С-пептидтің бөлінуі сандық түрде жүреді және бұл өнеркәсіптік масштабта мақсатты полипептидтер алу үшін мультимерикалық синтетикалық гендерді қолдануға мүмкіндік береді.
Қорытынды
Радикалды және көптеген жағдайларда қант диабетімен ауыратын науқастардың өмірі мен жұмыс қабілеттілігін сақтаудың жалғыз әдісі - қазіргі кезде инсулин.
Инсулинді қабылдаған және клиникалық тәжірибеге енгізер алдында, І типті қант диабетімен ауыратын науқастардың ауруы басталғаннан бастап бір-екі жыл ішінде, ең нашарлататын диеталарды қолданғанына қарамастан, өлім нәтижесі күтілді.
I типті қант диабетімен ауыратын науқастарға инсулин препараттарымен өмір бойы алмастыратын терапия қажет. Кез-келген себепке байланысты инсулинді тұрақты қабылдауды тоқтату асқынулардың тез дамуына және науқастың тез өліміне әкеледі.
Қазіргі уақытта қант диабетінің таралуы жүрек-тамыр жүйесі аурулары мен қатерлі ісіктерден кейін үшінші орында. Дүниежүзілік денсаулық сақтау ұйымының мәліметі бойынша, ересектер арасында қант диабетінің таралуы әлемнің көптеген аймақтарында 2-5% құрайды және әрдайым жоғарылайды.
1. науқастардың саны екі есе дерлік өсті Инсулинге тәуелді пациенттердің саны, денсаулық сақтау саласындағы айқын ілгерілеушілікке қарамастан, жыл сайын артып келеді және қазіргі уақытта Ресейде тек 2 миллион адам тұрады.
Инсулинді өндірудің ең перспективті әдістері гендік инженерия әдістері болып табылады. Гендік-инженерлік инсулин А және В тізбегін бөлек өндіруші штамдарды және молекуланың кейіннен бүктелуін қолдана отырып алынады, содан кейін изоформалар бөлініп, E. Coli жасушаларында проинсулин синтезі трипсинмен және карбоксепептидазмен және жергілікті инсулин өндірумен жүзеге асырылады.
Гендік-инженерлік инсулиннің отандық препараттарын құру диабетпен ауыратын миллиондаған адамдардың өмірін сақтау үшін ресейлік диабетологияның көптеген мәселелерін шешуге жаңа мүмкіндіктер ашады.
Әдебиет
Балаболкин М.И., Клебанова Е.М., Креминская В.М. Қант диабеті: диагностика мен емдеудің заманауи аспектілері / Дәрігер, ред. Г.Л.Вышковский.-2005.- М .: РЛС-2005, 2004.- 960 б.
Гавриков, А.В. Адамның рекомбинантты интерферондарының заттардың биотехнологиялық өндірісін оңтайландыру: дис. ... шам. биол. Ғылымдар - М, 2003
Гендік-инженерлік инсулин. Бифункционалдылық принципін қолдана отырып, хроматографиялық бөлудің тиімділігін арттыру. / Романчиков А.Б., Якимов С.А., Клюшниченко В.Е., Арутунян А.М., Вульфсон А.Н. // Биоорганикалық химия, 1997 - 23, № 2
Глик Б., Пастернак Дж. Биотехнологиялық әдістердің қолданылуын бақылау // Б. Глик, Дж.Парснип / Молекулалық биотехнология = Молекулалық биотехнология. - М.: Мир, 2002. - С. 517-532. - 589 б.
Глик Б., Пастернак Дж. Молекулалық биотехнология. Принциптер мен қолдану. М .: Мир, 2002.
Дэвис Р., Ботштайн Д, Рот Дж. Гендік инженерия әдістері. Бактериялардың генетикасы // Р.Дэвис, Д. Ботштейн, Дж.Рот / Пер. ағылшын тілінен.-М .: Мир.- 1984.- 176 б.
Ермишин А.П.Генетикалық түрлендірілген ағзалар: мифтер мен шындық / А.П.Ермишин // Мн .: Техналогалия.- 2004.- 118 б.
Фармацевтикалық биотехнология негіздері: Оқулық / Т.П. Пришеп, В.С. Чучалин, К.Л. Зайков, Л.К. Михалева. - Ростов-на-Дону: Финикс, Томск: NTL баспасы, 2006.
Патрушев Л.И. Жасанды генетикалық жүйелер. // Л.И.Патрушев / М .: Наука.- 2004.
Романчиков, А.Б. Гендік-инженерлік инсулин. Бифункционалдылық принципін қолдана отырып, хроматографиялық бөлудің тиімділігін арттыру. / Ә.Б. Романчиков және басқалар.
// Биоорганикалық химия. 1997. № 2. б. 23
Рыбчин В.Н. Гендік инженерия негіздері // В.Н. Рыбчин / 2-ші басылым, қайта қаралған. және қосу: ЖОО-ға арналған оқулық. SPb .: SPbSTU баспасы. - 2002 .-- 522 с.
Щелкунов С. Н. Гендік инженерия // Щелкунов С. Н. / Новосибирск: Сиб. унив. Баспа, 2008.
Щелкунов, С.Н. Гендік инженерия: оқулық. жәрдемақы. - 2-ші бас., Ред. және қосыңыз. - Новосибирск: Сиб. унив. Баспа, 2004. - 496 б.
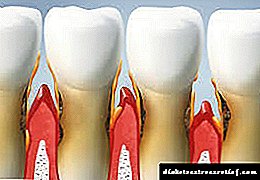
1. Инсулин молекуласындағы дисульфидті байланыстардың орналасуы.
2. Инсулин молекуласындағы амин қышқылы қалдықтарының орналасуы
Инсулиннің негізгі метаболикалық ферменттерге әсері
Бауыр бұлшықетінің май тінін белсендіру 1. Фосфодиэстераза 1. Фосфодиэстераза 1. LP-липаза
4. Пируватты дегидрогеназа кешені
4. Пируватты дегидрогеназа кешені
5. Фосфатаза гликоген синтаза және гликоген фосфорилаза
5. Гликоген синтаза фосфатаза b. Ацетил-КоА-карбоксилаза индукциясы 1. Глюкокиназа 1. Глицеральдегид фосфаты дегидрогеназа
6. Глюкоза-6-фосфатты дегидрогеназа репрессиясы Фосфоэнолпируват карбоксиназасы
Сур. 3 Лангерган аралдарының β-жасушаларында инсулин биосинтезінің сызбасы. ER - эндоплазмалық ретикулум. 1 - сигнал пептидінің пайда болуы, 2 - препросулин синтезі, 3 - сигнал пептидінің бөлінуі, 4 - просинулинді Голги аппаратына тасымалдау, 5 - проинсулиннің инсулинге және С-пептидке айналуы және инсулин мен С-пептидтің секрет түйіршіктеріне қосылуы, 6 - инсулин секрециясы және С пептиді.
4. Инсулинді өзінен бұрынғы адамдардан синтездеудің жалпы схемасы
Сур. 5 Екі бөлек тізбекті қалыптастыру арқылы инсулин синтезі
Адамның гендік-инженерлік инсулинін алу әдісі

Өнертабыс биотехнология саласына, атап айтқанда, қант диабетін емдеуде қолданылатын препараттарды өндіруге арналған гендік-инженерлік инсулинді өндіруге қатысты.
Бұл әдіс құрамында адам проинсулині бар гибридті ақуыз, Escherichia coli BL21 / pPINS07 (BL07) немесе Escherichia coli JM109 / pPINS07 өсіру арқылы жасушаларды ыдырату, гибридтік ақуыз бар инклюзивті денелерді бөлу арқылы жүзеге асырылады.
Әрі қарай, енгізу денелерін алдын-ала жуу, ақуызды бір уақытта еріту және буфердегі дисульфидті байланыстарды 5-10 м дитиотреитол және 1 мД ЭДТА көмегімен қалпына келтіру, ион алмастыру хроматографиясы арқылы қайта өзгертілген синтезделген ақуызды қайта құру және тазарту жүзеге асырылады.
Гибридті ақуыздың бөлінуі трипсин мен карбоксептидаза В-ның бірлескен гидролизі арқылы гибридті ақуыз, трипсин және карбоксептидаза В 4000: 0,6: 0.9 қатынасында болады.
Инсулинді тазарту гидрофобты хроматография немесе кері фазалы жоғары сұйықтықты хроматография, содан кейін гель фильтрациясымен, ал мырыш тұздары болған кезде кристалдану арқылы инсулинді оқшаулау арқылы жүзеге асырылады. Өнертабыс гендік-инженерлік инсулин алу процесін азайтуға және оның шығарылуын арттыруға мүмкіндік береді.
Өнертабыс биотехнология саласына, атап айтқанда, қант диабетін емдеуде қолданылатын препараттарды өндіруге арналған гендік-инженерлік инсулинді өндіруге қатысты.
Қазіргі диабетологияның негізгі жетістіктері мен Дүниежүзілік денсаулық сақтау ұйымының ұсыныстарына сүйене отырып, Еуропа елдері 2001 жылға қарай адам инсулинін қолдануға көшуді аяқтады. Осыған байланысты ДНҚ-рекомбинантты технологияны қолдана отырып инсулин алу әдістерін әзірлеу - кезек күттірмейтін мәселе.
Гендік-инженерлік инсулинді өндірудің белгілі әдісі, ол протецулин өндіретін E. Coli штамын өсіруден тұрады, оның құрамында стафилококк ақуызының A синтетикалық IgG екі синтетикалық домендерінің тізбегі бар.
Бұл әдіс бактериалды жасушаларды жою, проинсулині бар Таурус индукциясын алу, проинсулиннің тотықтырғыш сульфитолизі, оның қайта түзілуі, протеолиттік ферменттермен проинсулинді тазарту және ақуызды тазарту-ақуызды ақуызды тазарту және проинсулин ферменттерімен проинсулинді тазарту, проинсулиннің тотығу сульфитолизі, протинулиннің тотығу сульфитолизі. хроматография (Нилсон Дж. Джонассон П., Самуэлссон Э., Стахл С., Ухлен М. «Адам инсулинін және оның С-пептидін біріктірілген өндіру», Биотехнология журналы, 1996 ж., 48-бет, 241-250-беттер) .
Бұл әдістің кемшіліктері өнімнің қымбаттығы және мақсатты өнімде болуы мүмкін инсулинді жуғыш зат өндірісінде қолдану болып табылады.
Адамның гендік-инженерлік инсулинін өндірудің белгілі әдісі, ол өндіруші штаммның жасушаларын өсіруден тұрады.
Coli DN5 a / pVK100, ультрадыбыстық ыдырау арқылы бактериалды жасушаларды жояды, центрифугалау арқылы суда еритін қоспалардан гибридтік ақуызды қамтитын жеке денелерді қосады, 8 M мочевина, 1 м дитиотреитол, 0,1 М Tris-HCl бар буферге қосу денелерін ерітеді. рН 8.0, 12-16 сағат ішінде.
Ерімейтін қоспалар центрифугалау жолымен алынады, содан кейін дитиотреитолдың концентрациясы 10 мМ дейін артады және дисульфидті байланыс 1 сағат ішінде 37 ° C-та қалпына келеді. Ерітінді 5 рет суық сумен сұйылтылды, рН 4,5 деңгейіне келтіріліп, 2 сағат бойы 4 ° С температурада тұнба түзілді.
Гибридті ақуыз бар тұнба центрифугалаумен бөлініп, қалпына келтірілді, рН 10-12 суық суда тез ериді, содан кейін ол 10 мМ глицин буферімен, рН 10,8 сұйылтылды және түнде 4 ° C температурада ұсталды. Ультрафильтрациядан кейін ерітінді Sephadex G-50 бағанында гель фильтрациясына ұшырады және 10 мМ глицин буферімен тазартылды.
Термоядролық ақуыз бар фракциялар жиналады, ультрафильтрацияланады және қатып кептіріледі. Алынған синтезделген ақуыз 10 мг / мл концентрациясына 0,08 М Tris-HCl буферінде ериді және трипсинмен және карбоксепептидаз В-мен бір уақытта жарылады (карбоксептидаза В: трипсин: синтез ақуызы 0.3: 1: 10) 37 30 минут бойы ° C.
Содан кейін изопропанолды 40% қосыңыз. Қоспа DEAE-Sephadex A-25 бағанында хроматографқа түсіріліп, 0,05 М Tris-HCl буферімен, рН 7,5 40% изопропанолмен натрий хлориді сызықты градиентімен 0-ден 0,1 м-ге дейін алынады.Изопропанол жойылғаннан кейін натрий хлориді концентрациясы. 25% дейін жоғарылаңыз, рН-ны 2,0-ге ауыстырыңыз және инсулин тұнбасын жинаңыз.
(Чен Дж.-Ц., Чжан Х.Т., Ху М. - Н., Танг Дж.Г., «Адамның инсулинді E. Coli жүйесінде көрсетілгендей лиз-адам проинсулинімен өндіру» прекурсор «қолданбалы биохимия және биотехнология, 1995, 55-т., 5-15 б.).
Бұл әдістің кемшіліктері гибридті ақуыздың бөлінуінде қолданылатын көптеген сорбент пен ферменттердің көп мөлшерін қажет ететін бастапқы кезеңдерде гельді сүзуді қолдануды қамтиды.
Гендік-инженерлік адам инсулинін өндірудің белгілі әдісі, соның ішінде Escherichia coli JM109 / pPINS07 өндіруші штаммын өсіру, бактерия жасушаларын ыдырау арқылы ыдырату, гибридті ақуыз бар инклюзивті денелерді бөлу, несепнәр мен дитиотреитол бар буферде еріту, жаңарған ақуызды тазарту. қоспалық қосылыстардың 40% изопропанолдағы жауын-шашын, содан кейін КМ-сепарозадағы хроматография, оның трипсинмен және карбоксептидаза В-мен жүйелі түрде бөлінуі трипсинолизі 0,3-0,1 М аммоний ацетаты буферлі рН 5.0-6.0, құрамында 6 М мочевинасы бар, ақуыз элюциясы бар 0-ден 0,5 М-ге дейін натрий хлориді сызықты градиенті бар хроматографта СП-Сепарозға түсірілген. буфер және карбоксептидаза В-мен бөлінгеннен кейін алынған инсулин фракциясы кері фазалы, жоғары өнімді сұйықтық хроматографиясымен тазартылды (ГПЛ РП № 2141531, MKI C12P 21/02, публ.). 1999)
Әдістің кемшіліктері гибридті ақуызды тазарту кезеңінде мочевина мен органикалық еріткіштердің едәуір мөлшерін қолдануды қамтиды.
Қант диабеті бойынша маман

Инсулинді қолданар алдында қант диабеті бар науқастың өмір сүру ұзақтығы 10 жылдан аспайтын. Бұл препараттың өнертабысы миллиондаған науқастарды құтқарды. Адамның гендік инженерия инсулині - ғылымдағы ең соңғы жетістік.
Көпжылдық қажырлы еңбектің нәтижесі
Гендік инженерлік (рекомбинантты) препарат ойлап тапқанға дейін инсулин ірі қара мен шошқаның ұйқы безінен бөлінген.
Фарфор инсулинінің адамнан айырмашылығы - бір ғана амин қышқылы
Препарат алудың бұл әдісінің кемшіліктері:
- биологиялық шикізатты сақтау мен тасымалдаудың күрделілігі,
- малдың жетіспеушілігі
- ұйқы безінің гормонын бөлуге және тазартуға байланысты қиындықтар,
- аллергиялық реакциялардың жоғары қаупі.
1982 жылы биореактордағы табиғи адам инсулинінің синтезделуімен жаңа биотехнологиялық дәуір басталды. Егер инсулин терапиясының басында ғалымдардың мақсаты науқастың өмірін сақтау болса, қазіргі уақытта жаңа препараттарды әзірлеу аурудың орнықты өтемақысына қол жеткізуге бағытталған. Ғылыми зерттеулердің негізгі мақсаты - қант диабетімен ауыратын науқастың өмір сапасын жақсарту.
Қазіргі заманғы технологиялар
Дәрінің түрлері, дайындау әдісіне байланысты:
| Генетикалық инженерия рекомбинант | Өндіріс үшін генетикалық модификацияланған E. coli қолданылады.
| Генетиктердің сүйіктісі - E. coli |
| Генетикалық түрлендірілген | Бастапқы материал - шошқа инсулині. Ол гендік инженерия әдісімен өзгертілген. | Гормондардың құрылымы |
| Синтетикалық | Жасанды синтезделген дәрілік зат, оның құрамында адам инсулиніне мүлдем ұқсас. | Дәрілік заттарды өндіру |
Дәрілерді қабылдағаннан кейін ағзада не болады?
Жасуша мембранасының рецепторымен байланысып, инсулин келесі процестерді жүзеге асыратын кешен түзеді:
- Жасушааралық глюкозаның тасымалын жақсартады және оның сіңуін жеңілдетеді.
- Глюкозаны өңдеуге қатысатын ферменттердің бөлінуіне ықпал етеді.
- Бауырда гликоген түзілу жылдамдығын төмендетеді.
- Май мен ақуыз алмасуын ынталандырады.
Тері астына енгізу жағдайында инсулин 20-25 минуттан кейін әрекет ете бастайды. Препараттың ұзақтығы 5-тен 8 сағатқа дейін. Одан әрі инсулиназа ферментімен бөлініп, несеппен шығарылады. Препарат плацентадан өтпейді және емшек сүтіне енбейді.
Гендік-инженерлік инсулин қашан тағайындалады?
Егер шұғыл көмек қажет болса
Гендік-инженерлік инсулин келесі жағдайларда қолданылады:
- 1 типті немесе 2 типті қант диабеті. Ол тәуелсіз емдеу ретінде немесе басқа препараттармен бірге қолданылады.
- Ауызша гипогликемиялық агенттерге қарсы тұруымен.
- Жүкті әйелдердегі қант диабетімен.
- Бүйректен және бауырдан асқынған жағдайда.
- Ұзартылған инсулинге ауысқанда.
- Операция алдындағы кезеңде.
- Өмірге қауіпті жағдайлар туындаған кезде (гиперосмолярлы немесе кетоацидотикалық кома).
- Төтенше жағдайларда (босанғанға дейін, жарақатпен).
- Егер терінің дистрофиялық зақымдануы болса (жаралар, фурункулоз).
- Инфекция фонында қант диабетін емдеу.
Адамның гендік-инженерлік инсулині жақсы төзімді және аллергиялық реакциялар туғызбайды, өйткені ол табиғи гормонға толықтай сәйкес келеді.
Үнемі бақылау маңызды!
Келесі жағдайларда дәрі тағайындауға тыйым салынады:
- қандағы қантты төмендету
- препаратқа жоғары сезімталдық.
Препарат тағайындалғаннан кейінгі алғашқы күндерде науқасты мұқият бақылау қажет.
Жанама әсерлері
Уртикария қауіпті! Квинкенің ісінуі!
Сирек жағдайларда, инсулинді қолданған кезде келесі асқынулар болуы мүмкін:
- аллергиялық реакциялар (зәр шығару, Квинкке ісіну, терінің қышуы),
- қандағы қанттың күрт төмендеуі (ағзаның препарат қабылдамауына байланысты немесе иммунологиялық қақтығыс туындаған жағдайда);
- бұзылған сана
- ауыр жағдайларда гипогликемиялық команың дамуы мүмкін,
- шөлдеу, құрғақ ауыз, летаргия, тәбет жоғалту,
- гипергликемия (препаратты инфекция немесе қызба аясында қолданғанда),
- бет қызаруы
- қабылдау аймағындағы жергілікті реакциялар (қышу, қышу, атрофия немесе тері астындағы майдың көбеюі).
Кейде препаратқа бейімделу ісіну және көру қабілетінің бұзылуы сияқты бұзылулармен бірге жүреді. Бұл көріністер, әдетте, бірнеше аптадан кейін жоғалады.
Дәріханадан гендік-инженерлік инсулинді қалай табуға болады?
Медицина парентеральді енгізуге арналған шешім түрінде қол жетімді:
| «Биосулин» | Әрекеттің орташа ұзақтығы |
| Актрапид | Қысқа әсер ететін инсулин |
| Генсулин | Бифазиялық дайындық (қысқа және орташа инсулиндердің үйлесімі) |
| Ринсулин | Жылдам эффект |
| Гумалог | Дәрі қабылдау үшін шприц-қалам қолданылады. |
Науқастың жеке ерекшеліктерін ескере отырып, инсулин препаратын таңдау қиын емес.
Пайдалану шарттары
Көбінесе инсулинді тері астына енгізу қолданылады.
Шұғыл жағдайларда препарат ішілік енгізіледі.
Науқастың жағдайы ауыр
Тіпті тәжірибесі бар диабетик препарат қолдану кезінде қате жіберуі мүмкін.
Асқынулардың алдын алу үшін:
- Қолданар алдында дәрі-дәрмектің жарамдылық мерзімін тексеріңіз.
- Сақтау туралы ұсыныстарды орындаңыз: запас шишаларды тоңазытқышта сақтау керек. Әзірленген шишаны бөлме температурасында қараңғы жерде сақтауға болады.
- Дәрі-дәрмектің дұрыс мөлшерін есте сақтаңыз: дәрігердің рецептін қайта оқыңыз.
- Инъекциядан бұрын шприцтен ауаны шығару қажет.
- Тері таза болуы керек, бірақ өңдеу үшін алкогольді қолдану қажет емес, өйткені бұл препараттың тиімділігін төмендетеді.
- Инъекция үшін ең жақсы орынды таңдаңыз. Іштің тері астына енгізген кезде препарат тезірек әрекет етеді. Глютеальды қатпарға немесе иыққа енгізілгенде инсулинді баяу сіңіру.
- Беттің бүкіл аймағын қолданыңыз (жергілікті асқынулардың алдын алу). Инъекциялар арасындағы қашықтық кемінде 2 см болуы керек.
- Бұлшықетке түсу қаупін азайту үшін теріні қыртыстан ұстап алыңыз.
- Дәрі ағып кетпес үшін шприцті тері астына бұрышпен енгізіңіз.
- Асқазанға енгізгенде қысқа әсер ететін инсулин тамақтанудан 20 минут бұрын енгізіледі. Иық немесе бөкселерді таңдаған жағдайда - тамақтанудан отыз минут бұрын.
Басқа препараттармен біріктіру
Көбінесе қант диабетімен ауыратын науқас бірнеше дәрі қабылдайды. Басқа препараттармен үйлесу гендік-инженерлік инсулиннің терапиялық әсеріне әсер етуі мүмкін.
Асқынулардың алдын алу үшін сіз білуіңіз керек:
| Қандағы қантты төмендету арқылы гендік-инженерлік инсулиннің әсерін арттырыңыз |
| Зәр шығару жолдарының инфекцияларын емдеуде қолданылатын танымал дәрі-дәрмек |
| Инсулин әсерін азайтыңыз |
| Назар аударыңыз! Диуретикалық |
Артық дозалану
Кейбір жағдайларда инсулинді қабылдау қандағы қанттың кенеттен төмендеуіне әкеледі. Мәселе көбінесе дозаны дұрыс таңдамауға байланысты туындайды.
Гипогликемияның бастапқы белгілері:
- әлсіздік
- терінің бозаруы
- мазасыздық жағдайы
- бас айналу
- ығыстыру
- қолдың, аяқтың, тілдің және еріннің ауруы,
- аяқ-қолды дірілдету
- суық тер
- қатты аштық сезімі
- бас аурулары.
Діріл; әл-ауқаттың кенеттен нашарлауы
Егер сіз осы белгілерді байқасаңыз, тез сіңетін көмірсулар бар нәрсені тез жеуіңіз керек. Бұл печенье, кәмпит, қант кесегі немесе ақ нан болуы мүмкін. Мұндай жағдайларда тәтті шай көмектеседі.
Егер жағдай нашарласа, жедел жәрдем шақыру керек. Гипогликемия команың пайда болуына немесе науқастың өліміне әкелуі мүмкін.
Рекомбинантты инсулин қауіпті ме?
Сәлем Рекомбинантты инсулиннің табиғидан еш айырмашылығы жоқ. Оны алу үшін генетикалық түрлендірілген бактериялар қолданылады.
Гендік инженерия технологияларын қолдана отырып, инсулин гені бар рекомбинантты ДНҚ E. coli клеткасына енгізіледі. Генетикалық түрлендірілген организмдер көбейіп, гормон шығарады. Препарат өте тиімді және жоғары дәрежеде тазартылған.
Инсулин II бөлім. Микробиологиялық инсулин өндірісі

аффинициялық компонент - гибридті ақуыздың оқшаулануын айтарлықтай жеңілдетеді.
Бұл жағдайда екі компонент бір уақытта гибридті ақуыздың құрамында болуы мүмкін.
Сонымен қатар, гибридті ақуыздарды құру кезінде көп өлшемділік принципін қолдануға болады (яғни, гибридті ақуызда мақсатты полипептидтің бірнеше көшірмесі болады), бұл мақсатты өнімнің шығымдылығын едәуір арттыра алады.
2 проинсулиннің E. coli жасушаларында көрінісі.
Жұмыста авторлар метиониннің қалдықтары арқылы N-терминалына сызылған проинсулин мен Staphylococcus aureus ақуыз фрагменттерінен тұратын гибридті ақуызды білдіретін плазмидаға енгізілген нуклеотидті реттілікпен JM 109 N1864 штаммды қолданды.
Рекомбинантты штамм жасушаларының қаныққан биомассасын өсіру оқшаулау және дәйекті түрде өзгеруі инсулинге әкелетін гибридті ақуызды өндіруді бастайды.
Зерттеушілердің тағы бір тобы адам проинсулинінен тұратын метиониннің қалдықтары арқылы біріктірілген бактериалды экспрессивті жүйеде рекомбинантты ақуыз алды. Ни-агароз бағаналарында хелат хроматографиясын қолдану арқылы оқшауланған және цианоген бромидімен сіңірілген.
Ион алмасу хроматографиясы арқылы тазартылған проинсулинді анионды шайырмен және РП (кері фаза) HPLC-мен салыстыру және масс-спектрометриялық талдау, адамның проинсулинінің дисульфидті көпіріне сәйкес келетін дисульфидті көпірлердің болуын көрсетті. Мақалада прокариот жасушаларында генетикалық инженерия арқылы адам инсулинін өндірудің жаңа, жетілдірілген әдісін жасау туралы баяндалады. Авторлар нәтижесінде пайда болған инсулиннің құрылымы мен биологиялық белсенділігі ұйқы безінен оқшауланған гормонмен бірдей екенін анықтады.
Жақында генетикалық инженерия көмегімен рекомбинантты инсулинді алу процедурасын жеңілдетуге көп көңіл бөлінді. Сонымен, авторлар проинсулиннің N-терминалына лизиннің қалдықтары арқылы бекітілген интерлейкин 2-нің жетекші пептидінен тұратын синтезделген ақуыз алды.
Ақуыз тиімді түрде көрсетілді және инклюзивті денелерге локализацияланды. Оқшауланғаннан кейін ақуыз трипсинмен инсулин мен С-пептид алу үшін сіңірілді. Зерттеушілердің тағы бір тобы дәл осылай әрекет етті.
Проинсулин мен стафилококктың екі синтетикалық домендерінен тұратын синтетикалық ақуыз IgG байланыстыратын ақуыз қосылу денелерінде локализацияланған, бірақ жоғары дәрежеде көрініс тапқан. Ақуыз IgG көмегімен туыстық хроматография арқылы оқшауланып, трипсинмен және карбоксептидаза В-мен өңделді.
Алынған инсулин мен С-пептидті HPLC RP тазартты. Ерітілген құрылымдарды құру кезінде тасымалдаушы ақуыз мен мақсатты полипептидтің массалық қатынасы өте маңызды.
Осылайша, жұмыс термоядролық құрылымдардың құрылысын сипаттайды, онда адам сарысуы альбуминін байланыстыратын белок тасымалдаушы полипептид ретінде пайдаланылды. Оған бір, үш және жеті С-пептидтер қосылды.
С-пептидтер Sfi I шектеу учаскесін алып жүретін амин қышқылы кеңейткіштері мен белокты трипсинмен кейіннен бөлу үшін аралықтың басында және соңында екі аргинин қалдықтарын қолдана отырып, құйрық негізінде қосылды. Бөлінетін өнімдердің HPLC көрсеткендей, С-пептидтің бөлінуі сандық болып табылады және бұл өнеркәсіптік масштабта мақсатты полипептидтерді алу үшін мультимериялық синтетикалық гендерді қолдануға мүмкіндік береді.
Жұмыста Arg32Tyr алмастыруынан тұратын проинсулин мутантының дайындалуы сипатталған. Бұл ақуыз трипсинмен және карбоксептидаза В-мен біріккенде, тирозиннің қалдықтары бар инсулин және С-пептид түзілді. Соңғысы, 125I таңбаланғаннан кейін, радиоиммуноақпаратта белсенді қолданылады. 3 Инсулинді тазарту.
Дәрілік заттарды өндіруге арналған инсулин жоғары тазалықта болуы керек. Сондықтан өндірістің әр кезеңінде алынған өнімдердің тазалығын жоғары тиімді бақылау қажет. Бұрын RP және IO (ион алмасу) HPLC проинсулин-S-сульфонат, проинсулин, жеке A- және B-тізбектерін және олардың S-сульфонаттарын сипаттау үшін қолданылған.
Флуоресцентті инсулин туындысына ерекше назар аударылады. Жұмыста авторлар инсулин өндірісінің барлық кезеңдерінде өнімдерді талдау кезінде хроматографиялық әдістердің қолданылуы мен ақпараттылығын зерттеді және алынған өнімдерді тиімді бөлу және сипаттау үшін хроматографиялық операциялар кестесін жасады.
Сонымен қатар, инсулиннің тазалығы мен мөлшерін анықтауға арналған процестерді автоматтандыру және жеделдету тәсілдері жасалуда.
Жұмыста сұйық хроматографияны инсулинді анықтау үшін электрохимиялық анықтаумен қолдану мүмкіндігі зерттелгені және Лангерган аралынан оқшауланған инсулинді спектрометриялық анықтаумен иммунофаксинділік хроматографиясы арқылы анықтау әдістемесі жасалған.
Жұмыста капиллярлық электрофорезді пайдаланып лазерлік флуоресценцияны анықтайтын инсулинді жылдам микрокредиттеуді қолдану мүмкіндігі зерттелді. Талдау фенилизотиоцианатпен (FITC) белгіленген инсулиннің белгілі мөлшерін және моноклоналды инсулин антиденелерінің Fab фрагментін қосу арқылы жасалады. Белгіленген және тұрақты инсулиндер Fab кешенімен бәсекеге қабілетті. FITZ таңбаланған инсулин және оның Fab құрамы 30 секундта бөлінеді.
Жақында көптеген жұмыстар инсулин алу әдістерін жетілдіруге, сондай-ақ оның негізінде дәрілік формаларды жасауға арналды.
Мысалы, АҚШ-та гепатосецепті инсулин аналогтары патенттелген, құрылымы А горизонталының 13-15 және 19 позициясында және В тізбегінің 16 позициясында әр түрлі амин қышқылдарының қалдықтарының енгізілуіне байланысты табиғи гормоннан ерекшеленеді.
Алынған аналогтар қант диабетін емдеуде әртүрлі парентеральды (көктамырішілік, бұлшықетішілік, тері астындағы), интраназальды мөлшерде немесе имплантацияда қолданылады. Инъекцияларсыз енгізілетін дәрілік формаларды құру ерекше өзектілік болып табылады.
Жұмыста протеолитикалық фермент тежегіштерімен модификацияланған полимер гидрогелінің көлемінде иммобилизацияланған инсулин енгізілетін ауызша қабылдауға арналған макромолекулярлық жүйенің құрылуы туралы баяндалады. Мұндай препараттың тиімділігі тері астына енгізілген жергілікті инсулиннің тиімділігінің 70-80% құрайды.
Тағы бір жұмыста препарат инсулинді эритроциттермен бір сатылы инкубациялау арқылы байланысады, байланыстырғыш заттың қатысуымен 1-4: 100 қатынасында алынады.Авторлар препараттың қабылдау белсенділігі 1000 бірлік / г, ауызша қабылдағаннан кейін белсенділігі толық сақталуы және лиофилизацияланған түрінде бірнеше жыл сақталуы туралы хабарлайды.
Инсулинге негізделген жаңа дәрілер мен дәрілік формаларды жасаумен қатар, қант диабеті проблемасын шешудің жаңа тәсілдері жасалуда.
Осылайша, авторлар GLUT2 глюкозасын тасымалдаушы ақуыз cDNA ауыстырды, содан кейін HEP G2 жасушаларының толық өлшемді инсулинді кДНҚ-сы бар.
Алынған HEP G2 Insgl клондарында глюкоза қалыпты инсулин секрециясын ынталандырады және секрецияның басқа қоздырғыштарына секрецияны күшейтеді.
Иммуноэлектронды микроскопияда инсулині бар түйіршіктер морфологиялық тұрғыда Лангерган аралдарының б-жасушаларында түйіршіктерге ұқсас екенін анықтады. Гендік инженерия алған «жасанды б-жасушаны» 1 типті қант диабетін емдеу үшін қолдану мүмкіндігі қазіргі уақытта қатты талқылануда.
Практикалық мәселелерді шешумен қатар инсулиннің әсер ету механизмдері, сондай-ақ молекуладағы құрылымдық және функционалдық қатынастар зерттеледі. Зерттеу әдістерінің бірі инсулиннің әр түрлі туындыларын құру және олардың физика-химиялық және иммунологиялық қасиеттерін зерттеу 23, 24 болып табылады.
Жоғарыда айтылғандай, инсулин өндірудің бірқатар әдістері осы гормонды прекурсор (проинсулин) түрінде алуға негізделген, содан кейін инсулин мен С-пептидке ферментативті бөліну болады. Қазіргі уақытта С-пептид үшін биологиялық белсенділіктің бар екендігі көрсетілді, бұл оны инсулинмен қатар терапевтік мақсаттарда қолдануға мүмкіндік береді.
Осы серияның келесі мақалаларында С-пептидтің физика-химиялық және биологиялық қасиеттері, сондай-ақ оны дайындау әдістері қарастырылады.
Дәрілік заттарды өндірудегі биотехнология
STGh 20K нұсқасын алуға арналған әзірлемелер қызығушылық тудырады. Болашақ міндет - гормонның ұзаққа созылған әсерін алу үшін STH-тің әртүрлі формаларын ғана емес, сонымен қатар иммобилизацияланған STH алу және зерттеу. Ұзартылған әсерімен иммобилизацияланған STHch алудың өзіндік әдісі жасалды.
STH өндірумен қатар барлық түрлерге тән аденогипофиз гормондарын өндірудің біртұтас интеграцияланған технологиясы және олардың кейбір түрлерін ГСТ-тен алған. Гендік инженерия арқылы алынған STH (соматоген) емдік препаратын жасау бойынша мақсатты бағдарламаны жүзеге асыру үлкен маңызға ие.
Клиникалық тәжірибе көрсеткендей, қысқа бойлықты емдеуді оңтайландыру арқылы арсеналда әртүрлі технологиялармен немесе тіпті әдістермен алынған бірнеше ұқсас фармацевтикалық препараттар болуы керек (MF, Ausomatin, Somatogen).
HSCH бір препаратымен ұзақ мерзімді емдеу (жылдарға) оның ағзадағы сезімталдығының төмендеуіне әкеледі.
Бұл ішінара антиденелердің пайда болуының нәтижесі болуы мүмкін, бірақ негізгі себебін гормонды рецепторлар мен өңдеу деңгейінде іздеу керек.
GST-пен жұмыс, сонымен қатар жасырын гормондар мен олардың әртүрлі формаларын жан-жақты зерттеу табиғат жасаған жүйелерді зерттеуге және оларды жақсы түсінуге мүмкіндік береді. Организмде STH-тің әртүрлі нысандарының болуы олардың мақсатқа сай екендігін және, мысалы, клиникада мүмкін болатындығын көрсетеді.
STHch жаңа препараттарын жасау кезінде, ең алдымен STHch мономеріндегідей, гормонның табиғи табиғи формаларына назар аудару керек және оларды генетикалық инженерия арқылы кеңейту керек.
GST-тен STHch препараттарын өндіруде аденогипофиздің басқа гормондарын (LGH, FSHch, TTGch және басқалары) өндірудің кешенді өндірістік технологиясы сәтті енгізілуде. Жаңа жетілдірілген әдістерді (аффиниалды хроматография және т.б.) енгізу арқылы өндірісті оңтайландыру қажет.
интеграцияланған технологияны қолдана отырып, жоғары таза гормондарды алады.
Диагностика және биотехнология үшін аденогипофиз гормондарының иммуномикроанализі жиынтығын өндіруді және қолдануды кеңейту, әртүрлі масштабтағы стандартталған антиденелерді өндіруді жүзеге асыру, жаңа STHch препараттарын, соның ішінде иммобилизацияланған препараттарды жасау қажет.
STH ақуызға, майға және минералды зат алмасуға әсер етеді, жасуша деңгейінде мақсатты органсыз әрекет етеді және анаболикалық болып табылады, оны қалпына келтіру процестерін ынталандыру және түрлі ауруларды емдеу үшін қолдануға үлкен мүмкіндіктер береді. Осы мәселелерді кеңірек зерттеу, сонымен қатар STGch-тің әртүрлі өзгертілген нысандары мен нұсқаларын пайдалану мүмкіндігі - кезек күттірмейтін және келешегі зор міндет.
Биотехнологияда инсулин алу
Ұйқы безінің Лангерган аралындағы пептидті гормон инсулин диабеттің негізгі емі болып табылады. Бұл ауру инсулин тапшылығынан туындайды және қандағы глюкозаның жоғарылауымен көрінеді. Соңғы уақытқа дейін инсулин бұқаның және шошқаның ұйқы безінен алынды.
Препарат адам инсулинінен 1-3 аминқышқылын алмастырумен ерекшеленді, сондықтан аллергиялық реакциялар, әсіресе балаларда пайда болуы мүмкін. Инсулиннің кеңінен қолданылуы оның қымбаттығымен және шектеулі ресурстарымен шектелді.
Химиялық модификациялау арқылы жануарлардан инсулин адамнан бөлінбейтін болды, бірақ бұл өнім бағасының қосымша көтерілуін білдірді.
1982 жылдан бастап EliLilly E. coli A және B тізбектерін бөлек синтездеу негізінде гендік-инженерлік инсулин шығарады. Өнімнің өзіндік құны едәуір төмендеді, нәтижесінде алынған инсулин адам үшін бірдей. 1980 жылдан бастап, протеулин генін клондау туралы, протеолиздің шектеулі протеолизімен жетілген пішінге айналатын гормонның прекурсоры туралы баспасөзде хабарлар пайда болды.
Инкапсуляция технологиясы қант диабетін емдеуде де қолданылады: науқастың денесіне бір рет енгізілген капсуладағы ұйқы безі жасушалары жыл ішінде инсулин шығарады.
Біріктірілген генетика фолликулды ынталандыратын және лютеинизациялайтын гормондарды шығарды. Бұл пептидтер екі қосалқы бөліктен тұрады. Күн тәртібінде жүйке жүйесінің олигопептидті гормондарының - 5 аминқышқылдарының қалдықтарынан құрылған энкефалиндер мен морфиннің аналогтары сияқты эндорфиндердің өнеркәсіптік синтезі тұр.
Ұтымды қолданған кезде бұл пептидтер ауырсынуды жеңілдетеді, жақсы көңіл-күй қалыптастырады, тиімділікті арттырады, зейінді жақсартады, есте сақтау қабілетін жақсартады, ұйқы мен оятуды реттейді
Гендік инженерия әдістерін сәтті қолданудың мысалы - пептидті басқа гормон - соматостатин үшін жоғарыда сипатталған гибридті ақуыз технологиясын қолдану арқылы p-эндорфин синтезі.
Адамның инсулинін алу әдістері:
Тарихи тұрғыдан, терапевтік мақсаттар үшін инсулин алудың алғашқы әдісі - бұл гормонның аналогтарын табиғи көздерден (ірі қара мен шошқаның ұйқы безінің аралы) оқшаулау.
Өткен ғасырдың 20-жылдарында ірі қара және шошқа етінің инсулиндері (құрылымы мен амин қышқылдарының құрамы бойынша адам инсулиніне жақын) адам ағзасында адам инсулинімен салыстырмалы түрде белсенділік танытатыны анықталды. Осыдан кейін бұқа немесе шошқа инсулині І типті қант диабеті бар науқастарды емдеу үшін қолданылды.
Алайда, біраз уақыттан кейін, кейбір жағдайларда мал мен фарфор инсулиніне антиденелер адам ағзасына жинала бастайды, осылайша олардың әсерін жоққа шығарады.
Екінші жағынан, инсулин алудың осы әдісінің артықшылықтарының бірі шикізаттың болуы (мал мен шошқа етінің инсулинін көп мөлшерде алуға болады), бұл адам инсулинін шығарудың алғашқы әдісін дамытуда шешуші рөл атқарды.Бұл әдіс жартылай синтетикалық деп аталады.
Адам инсулинін өндірудің бұл әдісінде шикізат ретінде шошқа инсулині қолданылды. В тізбегінің C-терминалы октапептиді тазартылған фарс инсулинінен бөлініп алынды, содан кейін адам инсулинінің С-терминалы октапептиті синтезделді.
Содан кейін ол химиялық жолмен бекітілді, қорғаныш топтары алынып, нәтижесінде алынған инсулин тазартылды. Инсулин алудың осы әдісін сынау кезінде адам инсулиніне алынған гормонның толық сәйкестігі көрсетілді.
Бұл әдістің басты жетіспеушілігі - алынған инсулиннің жоғары құны (қазірдің өзінде, октапептидтің химиялық синтезі, әсіресе өнеркәсіптік ауқымда қымбат рахат).
Қазіргі уақытта адам инсулині негізінен екі жолмен алынады: синтетикалық-ферментативті әдіспен және гендік инженерия әдісімен фарфор инсулинін модификациялау арқылы.
Бірінші жағдайда әдіс Ala30Thr B тізбегінің C-терминалында шошқаның инсулині бір инсульттегі адам инсулинінен ерекшеленетіндігіне негізделген.
Аланинді треонинмен алмастыру аланиннің ферментті-катализденген бөлінуімен және оның орнына реакциялық қоспада көп мөлшерде болатын карбокси тобымен қорғалған треонин қалдықтарын қосу арқылы жүзеге асырылады. Қорғаныс O-терт-бутил тобынан бөлінгеннен кейін адам инсулині алынады.
Инсулин рекомбинантты ДНҚ технологиясын қолдана отырып, коммерциялық мақсатта алынған алғашқы ақуыз болды. Адамның гендік-инженерлік инсулинін өндірудің екі негізгі әдісі бар.
Бірінші жағдайда екі тізбек үшін бөлек (әр түрлі өндіруші штамдар) алынады, содан кейін молекуланың бүктелуі (дисульфидті көпірлердің пайда болуы) және изоформалардың бөлінуі жүреді.
Екіншіден, гормонның белсенді формасына трипсинмен және карбоксептидаз В-мен ферментативті ас қорыту арқылы прекурсор (проинсулин) түріндегі өндіріс.
Қазіргі уақытта инсулинді дисульфидті көпірлердің дұрыс жабылуын қамтамасыз ететін прекурсор түрінде қабылдаған жөн (тізбектерді бөлек дайындау жағдайында, денатурацияның дәйекті циклы, изоформалардың бөлінуі және регенатурация жүзеге асырылады).
Екі тәсілмен де бастапқы компоненттерді жеке алуға болады (A- және B-тізбектері немесе проинсулин) және гибридті ақуыздардың бөлігі ретінде. А және В тізбегінен немесе проинсулиннен басқа гибридті ақуыздар:
1) тасымалдаушы ақуыз - гибридті ақуызды клетканың немесе культура ортасының периплазмалық кеңістігіне тасымалдауды қамтамасыз ететін,
2) жақындық компоненті - гибридті ақуыздың оқшаулануын едәуір жеңілдетеді.
Бұл жағдайда екі компонент бір уақытта гибридті ақуыздың құрамында болуы мүмкін. Сонымен қатар, гибридті ақуыздарды құру кезінде көп өлшемділік принципін қолдануға болады (яғни, гибридті ақуызда мақсатты полипептидтің бірнеше көшірмесі болады), бұл мақсатты өнімнің шығымдылығын едәуір арттыра алады.
E. coli жасушаларында проинсулиннің көрінісі.
Метиониннің қалдықтары арқылы оның N-терминалына бекітілген сызықты проинсулин мен ақуыз фрагментінен тұратын стафилококк ауруынан тұратын синтезделген ақуызды білдіретін JM 109 N1864 штаммы қолданылды.
Рекомбинантты штамм жасушаларының қаныққан биомассасын өсіру оқшаулау және дәйекті түрде өзгеруі инсулинге әкелетін гибридті ақуызды өндіруді бастайды.
Зерттеушілердің тағы бір тобы адам проинсулинінен тұратын метиониннің қалдықтары арқылы біріктірілген бактериалды экспрессивті жүйеде рекомбинантты ақуыз алды. Ни-агароз бағаналарында хелат хроматографиясын қолдану арқылы оқшауланған және цианоген бромидімен сіңірілген.
Ион алмасу хроматографиясы арқылы тазартылған проинсулинді анионды шайырмен және РП (кері фаза) HPLC-мен салыстыру және масс-спектрометриялық талдау, адамның проинсулинінің дисульфидті көпіріне сәйкес келетін дисульфидті көпірлердің болуын көрсетті. Сондай-ақ, прокариот жасушаларында гендік инженерия арқылы адам инсулинін өндірудің жаңа, жетілдірілген әдісін жасау туралы баяндалады. Авторлар нәтижесінде пайда болған инсулиннің құрылымы мен биологиялық белсенділігі ұйқы безінен оқшауланған гормонмен бірдей екенін анықтады.
Жақында генетикалық инженерия көмегімен рекомбинантты инсулинді алу процедурасын жеңілдетуге көп көңіл бөлінді. Осылайша, лизиннің қалдықтары арқылы проинсулиннің N-терминалына қосылған интерлейкиннің жетекші пептидінен тұратын синтезделген ақуыз алынды. Ақуыз тиімді түрде көрсетілді және инклюзивті денелерге локализацияланды.
Оқшауланғаннан кейін ақуыз трипсинмен инсулин мен С-пептид алу үшін сіңірілді. Зерттеушілердің тағы бір тобы дәл осылай әрекет етті. Проинсулин мен стафилококктың екі синтетикалық домендерінен тұратын синтетикалық ақуыз IgG байланыстыратын ақуыз қосылу денелерінде локализацияланған, бірақ жоғары дәрежеде көрініс тапқан.
Ақуыз IgG-ге жақындықты хроматография арқылы оқшауланып, трипсинмен және карбоксептидаза В-мен сіңірілді. Алынған инсулин мен С-пептидті HPLC RP тазартты. Ерітілген құрылымдарды құру кезінде тасымалдаушы ақуыз мен мақсатты полипептидтің массалық қатынасы өте маңызды.
Термиялық конструкциялар құрылысы адам сарысуында альбумин байланыстыратын ақуыз тасымалдаушы полипептид ретінде қолданылатын жерде сипатталады. Оған бір, үш және жеті С-пептидтер қосылды.
С-пептидтер Sfi I шектеу учаскесін алып жүретін амин қышқылы кеңейткіштері мен белокты трипсинмен кейіннен бөлу үшін аралықтың басында және соңында екі аргинин қалдықтарын қолдана отырып, құйрық негізінде қосылды. Бөлінетін өнімдердің HPLC көрсеткендей, С-пептидтің бөлінуі сандық болып табылады және бұл өнеркәсіптік масштабта мақсатты полипептидтерді алу үшін мультимериялық синтетикалық гендерді қолдануға мүмкіндік береді.
Arg32Tyr алмастыруынан тұратын мутантты проинсулин алу. Бұл ақуыз трипсинмен және карбоксептидаза В-мен біріккенде, тирозиннің қалдықтары бар инсулин және С-пептид түзілді. Соңғысы, 125I таңбаланғаннан кейін, радиоиммуноақпаратта белсенді қолданылады.
Дәрілік заттарды өндіруге арналған инсулин жоғары тазалықта болуы керек. Сондықтан өндірістің әр кезеңінде алынған өнімдердің тазалығын жоғары тиімді бақылау қажет. Бұрын RP және IO (ион алмасу) HPLC проинсулин-S-сульфонат, проинсулин, жеке A- және B-тізбектерін және олардың S-сульфонаттарын сипаттау үшін қолданылған.
Флуоресцентті инсулин туындысына ерекше назар аударылады. Жұмыста авторлар инсулин өндірісінің барлық кезеңдерінде өнімдерді талдау кезінде хроматографиялық әдістердің қолданылуы мен ақпараттылығын зерттеді және алынған өнімдерді тиімді бөлу және сипаттау үшін хроматографиялық операциялар кестесін жасады.
Сонымен қатар, инсулиннің тазалығы мен мөлшерін анықтауға арналған процестерді автоматтандыру және жеделдету тәсілдері жасалуда.
Инсулинді анықтау үшін электрохимиялық анықтаумен RP сұйық хроматографиясын қолдану мүмкіндігі туралы зерттеулер жүргізіліп, Лангерган аралынан оқшауланған инсулинді иммуноафиниді хроматография көмегімен спектрометриялық анықтауда әдіснамасы жасалды.
Жұмыста капиллярлық электрофорезді пайдаланып лазерлік флуоресценцияны анықтайтын инсулинді жылдам микрокредиттеуді қолдану мүмкіндігі зерттелді.Талдау фенилизотиоцианатпен (FITC) белгіленген инсулиннің белгілі мөлшерін және моноклоналды инсулин антиденелерінің Fab фрагментін қосу арқылы жасалады. Белгіленген және тұрақты инсулиндер Fab кешенімен бәсекеге қабілетті. FITZ таңбаланған инсулин және оның Fab құрамы 30 секундта бөлінеді.
Гендік инженерлік инсулин

Инсулин неден жасалады деген сұрақ дәрігерлер мен фармацевттерді ғана емес, қант диабетімен ауыратын науқастарды, сондай-ақ олардың туыстары мен достарын қызықтырады.
Бүгінгі таңда адам денсаулығы үшін бұл ерекше және өте маңызды гормонды арнайы өңделген және мұқият тексерілген технологияларды қолдану арқылы әртүрлі шикізаттардан алуға болады. Дайындау әдісіне байланысты инсулиннің келесі түрлері бөлінеді:
- Шошқа еті немесе ірі қара, оны жануарлар өнімі деп те атайды
- Модификацияланған биосинтетикалық шошқа
- Генетикалық инженерлік немесе рекомбинантты
- Генетикалық түрлендірілген
- Синтетикалық
Шошқа етінің инсулині қант диабеті үшін ең ұзақ қолданылды. Оны қолдану өткен ғасырдың 20-жылдарында басталды.
Өткен ғасырдың 80-жылдарына дейін шошқа немесе жануарлардың жалғыз дәрі болғандығын атап өткен жөн. Оны алу үшін ұйқы безінің тіндері қолданылады.
Алайда бұл әдісті оңтайлы немесе қарапайым деп атауға болмайды: биологиялық шикізатпен жұмыс істеу әрдайым ыңғайлы емес, ал шикізаттың өзі жеткіліксіз.
Сонымен қатар, фарфор инсулинінің құрамы сау адам шығаратын гормонның құрамымен толығымен сәйкес келмейді: олардың құрылымында әртүрлі амин қышқылдарының қалдықтары бар. Ірі қара малдың ұйқы безі шығаратын гормондардың айырмашылықтары одан да көп, оларды жағымды құбылыс деп атауға болмайды.
Мұндай дайындықта таза көп компонентті субстанциядан басқа, проинсулин деп аталатын құрамы әрдайым болады, оны қазіргі заманғы тазарту әдістерімен бөлуге болмайды. Ол жиі аллергиялық реакциялардың көзіне айналады, әсіресе балалар мен қарттар үшін қауіпті.
Дәріханалар тағы бір рет қант диабетімен ауыратындарға ақша алғысы келеді. Қазіргі заманғы еуропалық есірткі бар, бірақ олар бұл туралы үндемейді. Бұл.
Осы себепті, әлемнің ғалымдары бұрыннан жануарлар шығаратын гормонның құрамын сау адамның асқазан безінің гормондарына толық сәйкестендіруге қызығушылық танытып келеді. Қант диабетін емдеудің фармакологиясы мен емдеудегі нақты бір жартылай синтетикалық препараттың пайда болуы аминқышқыл аланинді жануарлардың треонинмен алмастыру арқылы алынды.
Сонымен қатар, гормонды өндірудің жартылай синтетикалық әдісі жануарларға арналған препараттарды қолдануға негізделген. Басқаша айтқанда, олар жай ғана модификациядан өтіп, адамдар шығаратын гормондарға ұқсас болады. Олардың артықшылықтарының бірі - адам ағзасына үйлесімділік және аллергиялық реакциялардың болмауы.
Бұл әдістің кемшіліктеріне шикізаттың жетіспеушілігі және биологиялық материалдармен жұмыс жасау қиындықтары, сонымен қатар технологияның өзі де, нәтижесінде пайда болатын дәрілік заттың қымбаттығы да жатады.
Осыған байланысты қант диабетін емдеуге арналған ең жақсы дәрі-дәрмек генетикалық инженерия арқылы алынған рекомбинантты инсулин болып табылады.
Айтпақшы, оны көбінесе гендік-инженерлік инсулин деп атайды, осылайша оны алу әдісін көрсетеді, ал алынған өнім адам инсулині деп аталады, осылайша оның сау адамның ұйқы безі шығаратын гормондарға абсолютті сәйкестігін баса көрсетеді.
Гендік инженерлік инсулиннің артықшылықтарының бірі оның жоғары тазалығы мен проинсулиннің жетіспеушілігін, сонымен қатар аллергиялық реакциялар туғызбайтындығын және қарсы көрсетілімдері жоқ екенін де атап өткен жөн.
Жиі қойылатын сұрақ түсінікті: рекомбинантты инсулин неден жасалады? Бұл гормон ашытқы штамдары, сондай-ақ арнайы қоректік ортаға орналастырылған Escherichia coli арқылы шығарылатыны белгілі болды. Сонымен қатар, алынған заттың мөлшері соншалық, жануарлар органдарынан алынған препараттарды қолданудан толығымен бас тартуға болады.
Әрине, бұл жай Э.Коли туралы емес, гендік модификацияланған және құрамы мен қасиеттері сау адамның ұйқы безі жасушалары шығаратын гормонға ұқсас гендік-инженерлік инсулинді шығаруға қабілетті.
Гендік инженерлік инсулиннің артықшылығы оның адам гормонына абсолютті ұқсастығы ғана емес, сонымен қатар дайындықтың жеңілдігі, шикізаттың жеткілікті мөлшері және қол жетімді құны.
Дүние жүзіндегі ғалымдар рекомбинантты инсулин өндірісін қант диабетін емдеудегі нақты жетістік деп атады. Бұл ашылудың маңыздылығы соншалықты үлкен, сондықтан оны асыра бағалау қиын.
Қазіргі уақытта бұл гормонға деген қажеттіліктің 95% -ы гендік-инженерлік инсулиннің көмегімен қанағаттандырылатындығын атап өту жеткілікті.
Сонымен қатар, бұрын есірткіге аллергиясы бар мыңдаған адамдар қалыпты өмір сүруге мүмкіндік алды.
Менде 31 жыл диабет болды. Ол қазір сау. Бірақ, бұл капсулалар қарапайым адамдар үшін қол жетімді емес, дәріханаларды сатқысы келмейді, бұл олар үшін тиімді емес.
Адамның инсулині қалай жұмыс істейді
1 типті қант диабетін емдеуде адамның екі фазалы гендік-инженерлік инсулині қолданылады. Дәріханаларда ол ерітінді түрінде сатылады және «Сүйікті» белгісі бар. Аурудың екінші түрін, егер тағайындалған дәрі-дәрмектер диабетикке сәйкес келмесе, осындай препаратпен емдеуге болады.
Егер адамда диабеттік кома болса, гендік-инженерлік инсулин де қолданылады. Дәрігерлер қантты төмендететін таблеткалар мен терапевтік диета көмектеспеген кезде, қант диабеті диагнозы қойылған жүкті әйелдерге инъекцияны жиі тағайындайды.
Жалпы алғанда, генетикалық инженерияланған инсулиндер немесе ГМО босану кезінде, олар операция жасағанда немесе диабетпен ауыр жарақат алса қолданылады. Препарат тез әрекет ететін гормондарды қолдануға қауіпсіз ауысуға мүмкіндік береді.
- Инсулиннің бифазиялық гендік инженериясын қолданар алдында тест жасап, бұл дәрі науқасқа жарамды ма екенін анықтап алу керек. Егер диабетик гипогликемияны анықтаса, препаратты қолдану ұсынылмайды.
- Ерітіндінің әсер ету схемасы генетикалық инженерлік инсулин жасушалармен әрекеттеседі, бұл комплекстердің пайда болуына әкеледі. Жасушалар осы кешендерге енген кезде олар ынталандырылып, белсенді жұмыс істей бастайды. Нәтижесінде көбірек ферменттер өндіріледі.
- Бұл процесте глюкоза тез сіңеді, денеге енетін көмірсулар белсенді түрде өңделеді. Осылайша, бауыр глюкозаны ұзақ өндіреді, ақуыздарды тезірек сіңіруге болады.
Препараттың әрекет ету принципі дозаға, инсулин түріне, инъекциялық аймақты таңдауға байланысты. Кез-келген процедураны емдеуші дәрігермен келіскеннен кейін ғана жасау керек. Алғашқы инъекциялар медициналық бақылауда жасалады.
Препаратты қолдану бойынша ұсыныстар
Ұқсас немесе инсулинді бифазиялық адамның гендік инженериясы әртүрлі сауда атауларына ие. Сондай-ақ, гормондар әсер ету мерзіміне, ерітінді дайындау әдісіне байланысты өзгеруі мүмкін. Өнімдер инсулин түріне байланысты аталған.
Гендік-инженерлік инсулиндер Humudar, Vozulim, Actrapid сияқты дәрі-дәрмектердің құрамына кіреді. Инсуран, Генсулин. Бұл мұндай дәрі-дәрмектердің толық тізімі емес, олардың саны өте үлкен.
Жоғарыда аталған дәрі-дәрмектердің барлығы ағзаға әсер ету тұрғысынан әр түрлі болады.ГМО бірнеше сағатқа созылуы мүмкін немесе бүкіл күн бойы белсенді бола алады.
Екі фазалы аралас препараттар құрамына препараттың әсер ету мерзімін өзгертетін белгілі бір құрамдас бөліктерді қосатын дәрілер жатады.
- Мұндай препараттар генетикалық жолмен алынған гормондарды қосқанда, қоспалар түрінде сатылады.
- Бұл қаражатқа Микстард, Инсуман, Гансулин, Генсулин кіреді.
- Дәрі-дәрмектер күніне екі рет, тамақтанудан жарты сағат бұрын қолданылады. Мұндай жүйені қатаң сақтау керек, өйткені гормон тамақтану кезеңіне тікелей байланысты.
Адамның инсулинін гендік әдіспен шығарудың орташа уақыты бар препарат алынады.
- Ерітінді 60 минут ішінде күшіне енеді, бірақ ең жоғары белсенділік сәті инъекциядан алты-жеті сағат өткен соң байқалады.
- Дәрі 12 сағаттан кейін денеден толығымен шығарылады.
- Мұндай препараттарға Insuran, Insuman, Protafan, Rinsulin, Biosulin кіреді.
Сондай-ақ, организмге қысқа уақыт әсер ететін ГМО бар. Оларға инсулин Actrapid, Gansulin, Humulin, Insuran, Rinsulin, Bioinsulin кіреді. Мұндай инсулиндер екі-үш сағаттан кейін белсенді фазаға ие, препараттың әсер етуінің алғашқы белгілері инъекциядан кейін жарты сағат ішінде көрінеді.
Инсулинді енгізер алдында ГМО-ны мөлдірлік пен сұйықтықта бөгде заттардың болмауын тексеру қажет. Егер медицинада бөтен заттар, бұлшықет немесе жауын-шашын пайда болса, шишаны тастау керек - дәрі қолдануға жарамсыз.
Пайдаланылған инсулин бөлме температурасында болуы керек. Егер диабетте инфекциялық ауру, қалқанша безінің дисфункциясы, Аддисон ауруы, гипопититаризм және созылмалы бүйрек аурулары болса, гормонның мөлшерін түзету керек.
Гипогликемия ұстамалары препараттың дозаланғанда болуы мүмкін, егер инсулиннің жаңа түріне ауысқан болса, тамақты өткізіп жіберуге немесе физикалық шамадан тыс жүктемеге байланысты болады. Сонымен қатар, гормонға деген қажеттілікті төмендететін аурулар болуы мүмкін - бүйрек аурулары, бауыр аурулары, қалқанша безінің төмендеуі, бүйрек үсті безі және гипофиз.
- Қандағы қанттың күрт төмендеуі инъекция аймағының өзгеруімен мүмкін. Сондықтан инсулиннің бір түрінен ақылға қонымды және тек дәрігермен келіскеннен кейін ғана ауысу керек.
- Егер диабетик қысқа әсер ететін инсулинді қолданса, кейде инъекция орнында майлы тіннің мөлшері азаяды немесе керісінше көбейеді. Бұған жол бермеу үшін әр түрлі жерлерде инъекция жасау керек.
Жүкті әйелдер жүктіліктің әр түрлі триместрлерінде инсулинге деген қажеттілік әртүрлі болуы мүмкін екенін білуі керек. Мұны істеу үшін сіз глюкометрмен күнделікті қандағы қант сынағын жүргізуіңіз керек.
Инсулиннің адам ағзасына әсері осы мақалада бейнеде егжей-тегжейлі сипатталған.
1. Инсулиннің құрылымы мен функциялары 5
1.1. 5 инсулин молекуласының құрылымы
1.2. Инсулиннің биологиялық маңызы 7
1.3. Инсулин биосинтезі 8
2. Инсулиннің генетикалық инженериясы 10
2.1. Дәрілерді синтездеу үшін гендік инженерлік әдістерді қолдану 10
2.2. Генетикалық инженерия әдістері 11
2.3. Инсулиннің гендік инженериясы 14

Қорытынды 18
Артық дозалану белгілері
Инсулинді қолдану кезінде дәрігердің ұсыныстарын орындау және тағайындалған препараттың нақты дозасын сақтау маңызды.
Ережені сақтамаған және артық дозаланған жағдайда, диабетик қатты ауыра бастайды, құрысулар, аштық, тершеңдік, жүрек соғуы, адам қатты жұмыс істейді, ашуланады. Бүкіл денеде қалтырау және діріл байқалуы мүмкін.
Мұндай белгілер қан глюкозасының төмендеу белгілеріне өте ұқсас.Симптомдардың жұмсақ сатысымен диабетик өз бетінше мәселені шешіп, жағдайын жақсарта алады. Мұны істеу үшін кәмпит немесе қант бар кез-келген басқа тәтті өнімді жеп қойыңыз.
- Егер диабеттік кома пайда болса, олар декстроза ерітіндісін қолданады, препарат адам есіне түскенге дейін көктамыр ішіне енгізіледі. Алғашқы күдікті белгілерде жедел жәрдем шақыру керек, ол науқасты шұғыл әдістермен өмірге әкеледі.
- ГМО қолданғаннан кейін жанама әсерлер ретінде адамда терінің қышуы түрінде бөртпелер пайда болады, дененің бөліктері ісіп кетеді, қан қысымы күрт төмендейді, қышу және тыныс алу мүмкін. Бұл дәріге аллергиялық реакция, ол біраз уақыттан кейін медициналық араласусыз өздігінен жоғалып кетуі мүмкін. Егер жағдай жалғаса берсе, дәрігермен кеңесу керек.
- Инсулин препаратын қабылдаған алғашқы күндерде диабетпен ауыратындар денені жиі сусыздандырады, адамда сұйықтық жетіспейді, тәбет нашарлайды, аяқ-қолдарда ісіну пайда болады, үнемі ұйқышылдық сезіледі. Мұндай белгілер әдетте тез кетеді және қайталанбайды.
Пікірлер мен пікірлер
Менде 2 типті қант диабеті бар - инсулинге тәуелді емес. Досыңыз қандағы қантты DiabeNot-пен төмендетуге кеңес берді. Интернет арқылы тапсырыс бердім. Қабылдау басталды.
Мен қатал емес диетаны ұстанамын, әр таңертең жаяу 2-3 шақырым жүре бастадым. Соңғы екі аптаның ішінде мен таңертең таңертеңгі сағат 9.3-тен 7.1-ге, ал кешегі тіпті 6-ға дейін қанттың біртіндеп төмендегенін байқадым.
1! Мен профилактикалық курсты жалғастырамын. Мен жетістіктер туралы жазылымнан бас тартамын.
Маргарита Павловна, мен қазір Диабеноттың үстінде отырмын. SD 2. Менде шынымен диета және серуендеуге уақыт жоқ, бірақ мен тәттілер мен көмірсулардан бас тартпаймын, менің ойымша, XE, бірақ жасына байланысты қант әлі де жоғары.
Нәтижелер сіздікіндей жақсы емес, бірақ 7.0 қант бір апта ішінде шықпайды. Қантты қандай глюкометрмен өлшейсіз? Ол сізге плазманы немесе бүкіл қанды көрсете ме? Мен дәрі қабылдаудан алынған нәтижелерді салыстырғым келеді.
Осындай ақпараттық хабарлама үшін көп рахмет.
Инсулиннің гендік инженериясы

Адам өзін сау сезінуі үшін ағзадағы инсулин деңгейін бақылау керек. Бұл гормон глюкозаның қанда жиналмауы үшін жеткілікті болуы керек. Әйтпесе, метаболикалық бұзылулар болған жағдайда дәрігер диабет диагнозын қояды.
Қант диабетінің дамыған кезеңіндегі терапия - бұл организм табиғи жолмен өндіре алмайтын инсулиннің жетіспейтін концентрациясын қалпына келтіру. Ол үшін еритін инсулин қолданылады, ол адамның генетикалық инженирленуіне ұқсас. Ұйқы безі осындай гормонды өндіруге жауап береді.
Инсулинді өндіру үшін табиғи гормон шығару технологиясы ғана емес, өндірушілер жасанды түрде алынған модификацияланған инсулинді де пайдаланады. «Солубилис» деген препарат еритін ретінде көрсетілген.
Дәрілердің түрлері
Ұқсас немесе инсулинді бифазиялық адамның гендік инженериясы әртүрлі сауда атауларына ие. Сондай-ақ, гормондар әсер ету мерзіміне, ерітінді дайындау әдісіне байланысты өзгеруі мүмкін. Өнімдер инсулин түріне байланысты аталған.
Гендік-инженерлік инсулиндер Humudar, Vozulim, Actrapid сияқты дәрі-дәрмектердің құрамына кіреді. Инсуран, Генсулин. Бұл мұндай дәрі-дәрмектердің толық тізімі емес, олардың саны өте үлкен.
Жоғарыда аталған дәрі-дәрмектердің барлығы ағзаға әсер ету тұрғысынан әр түрлі болады. ГМО бірнеше сағатқа созылуы мүмкін немесе бүкіл күн бойы белсенді бола алады.
Екі фазалы аралас препараттар құрамына препараттың әсер ету мерзімін өзгертетін белгілі бір құрамдас бөліктерді қосатын дәрілер жатады.
- Мұндай препараттар генетикалық жолмен алынған гормондарды қосқанда, қоспалар түрінде сатылады.
- Бұл қаражатқа Микстард, Инсуман, Гансулин, Генсулин кіреді.
- Дәрі-дәрмектер күніне екі рет, тамақтанудан жарты сағат бұрын қолданылады. Мұндай жүйені қатаң сақтау керек, өйткені гормон тамақтану кезеңіне тікелей байланысты.
Адамның инсулинін гендік әдіспен шығарудың орташа уақыты бар препарат алынады.
- Ерітінді 60 минут ішінде күшіне енеді, бірақ ең жоғары белсенділік сәті инъекциядан алты-жеті сағат өткен соң байқалады.
- Дәрі 12 сағаттан кейін денеден толығымен шығарылады.
- Мұндай препараттарға Insuran, Insuman, Protafan, Rinsulin, Biosulin кіреді.
Сондай-ақ, организмге қысқа уақыт әсер ететін ГМО бар. Оларға инсулин Actrapid, Gansulin, Humulin, Insuran, Rinsulin, Bioinsulin кіреді. Мұндай инсулиндер екі-үш сағаттан кейін белсенді фазаға ие, препараттың әсер етуінің алғашқы белгілері инъекциядан кейін жарты сағат ішінде көрінеді.
Мұндай препараттар алты сағаттан кейін толығымен шығарылады.
Қант диабеті үшін гендік-инженерлік инсулинді қолдану

Адамның гендік-инженерлік инсулині - бұл ұйқы безін шығаратын инсулинге арналған жалпы гормонды ауыстыру. Синтездеу үшін адамның генетикалық модификацияланған гормоны ғана емес, сонымен бірге синтетикалық жолмен жасалған зат қолданылады. Препараттың тағы бір танымал нұсқасы - өзгертілген шошқа инсулинін қолдану, өйткені құрамы мен функциялары бойынша ол адамға ең жақын. Гендік инженерлік инсулин өндірісінің кестесі. Генетикалық инженерлік инсулинді гипогликемиялық сипаты бар ауызша препараттарға тұрақты реакция байқалған кезде, 1 типті қант диабеті үшін де, 2 типті қант диабеті үшін де қолдануға болады. Оны науқас команың белгілі бір түрлерінде болған кезде қолдануға болады. Егер жүкті әйел қант диабетімен ауыра бастаса, онда инженерлік инсулинді қолдануға рұқсат етіледі, бірақ диета глюкоза деңгейіне әсер етпесе ғана. Оны қолдану гипертермияны байқауға болатын инфекциялармен ауырған кезде ұсынылады. Гендік препараттар босану кезінде, операцияларда, жарақатта, метаболизмнің бұзылуында және инсулинге біртіндеп ұзақ әсер ету жағдайында қолдануда сәтті болады. Гормонды препараттың жекелеген элементтеріне жоғары сезімталдықпен және гипогликемиямен алмастыратын гендік препараттарды қолдануға тыйым салынады. Бұл түрдегі дәрілер жасуша мембраналарының белгілі бір рецепторларымен әрекеттесіп, олармен кешен түзеді. Ол жасушаларға енген кезде препараттың кешені жұмысқа әсер етіп, оны белсенді болуға және қосымша ферменттер шығаруға ынталандырады. Глюкоза деңгейі оның жасушалармен тез өңделуіне байланысты төмендейді. Осыдан кейін липогенез процесі, ақуыз өндірісі жеделдейді және бауырда глюкоза түзілу жылдамдығы төмендейді. Препараттың қолданылу мерзімі инъекция орнына, препарат түріне, мөлшеріне және адам ағзасының жеке реакциясына байланысты болады. Осы топта белгілі бір дәрі-дәрмектерді тағайындай алатын дәрігер ғана тағайындай алады. Препаратты қабылдаудың алғашқы кезеңінде пациент дәрігерлер препараттың қабылданбағанын білу үшін мұқият бақыланады. Адамның гендік-инженирленген инсулині Insuran, Insuman, Vozulim, Penfill, Biosulin, Gensulin, Actrapid, Rinsulin, Humulin, Humudar, Rosinsulin және басқалары сияқты танымал дәрілердің құрамында болады. Инсулиннің әртүрлі түрлері бар.Классификациялардың бірі препараттың қолданылу мерзіміне қатысты. Оның айтуынша, еритін инсулин қысқа және ұзақ әсер етуі мүмкін. Құрамында тез және ұзаққа созылатын әсер ететін құрамдас дәрілер бар (бифазиялық инсулин). Дәрі-дәрмектің бұл түрі қоспа деп аталады. Олардың арасында адам гормонының өзгеруімен жасалынатындар да бар. Екі фазалы инсулин - Микстард, Гансулин, Инсуман, Гумулин және Генсулин. Оларды күніне екі рет, тамақтанудан жарты сағат бұрын қолдану керек. Бұл екі фазалы инсулиннің қысқа әсер ететін затқа ие болуымен байланысты, оны қабылдау диетаға байланысты. Адам гормонының инженерлік аналогы орташа ұзақтығы бар дәрілердің қатарына жатады. Бұл еритін инсулин бір сағаттан кейін әрекет ете бастайды, ал белсенділігінің шыңы 7 сағаттан кейін пайда болады. 12 сағаттан кейін ол көрсетіледі. Осы топтың гендік-инженерлік препараты - Инсуман, Протафан, Гумулин, Ринсулин, Биосулин, Генсулин, Гансулин, Инсуран. Бұл топтың ішінде қысқа әрекеті бар адамның гендік-инженерлік есірткісі бар. Мысалы, бұларға Гансулин, Инсуран, Гумулин, Ринсулин, Генсулин, Биоинсулин және Актрапид жатады. Мұндай еритін инсулин жарты сағаттан кейін әрекет ете бастайды, ал оның белсенділігі бірнеше сағат ішінде ең жоғарғы деңгейге жетеді. Мұндай препараттар 6 сағат ішінде шығарылады. Гендік-инженерлік инсулині бар есірткі дозаланғанда, әлсіздік, ұйқышылдық, шаршағыштық, тітіркену, суық тердің шығарылуының жоғарылауы, дірілдеу, бозару, жүрек соғысы, бас ауруы, құрысулар және аштық болуы мүмкін. Мұның бәрі гипогликемия белгілері. Егер бұл ауру енді дами бастаса және оның ертерек, жеңіл сатысында болса, онда сіз барлық белгілерді өзіңіз алып тастай аласыз. Мұны істеу үшін сіз қантпен және көп мөлшерде көмірсулармен тамақтануыңыз керек, оны оңай сіңіруге болады. Глюкагон мен декстроза ерітіндісін ағзаға енгізуге болады. Егер адам комаға түсіп кетсе, онда жағдайды жақсартқанға дейін өзгертілген декстроза ерітіндісін енгізу керек. Кейбір адамдарда инсулині бар генетикалық модификацияланған препараттарды қолдануға аллергиялық реакциялар пайда болуы мүмкін. Симптомдарға есекжем, ісіну, күш жоғалту, төмен қан қысымы, ентігу, бөртпе, безгегі және қышу жатады. Кейбір жағдайларда гипогликемия және кома пайда болады. Адамның санасында және тіпті комада проблемалар туындауы мүмкін. Егер пациент дәрі-дәрмекті қабылдамаса, онда гипергликемия дамуы мүмкін. Бұл ағзадағы инфекциялық құбылыстардың пайда болуымен, сондай-ақ егер сіз диета ережелерін сақтамасаңыз, алдын-ала төмен дозаларға байланысты пайда болады. Кейбір жағдайларда науқаста препарат тағайындалған жерлерде липодистрофия дамуы мүмкін. Препаратты қолданудың басында ісік, судың болмауы, ұйқышылдық және тәбеттің бұзылуы мүмкін. Бірақ бұл құбылыстар уақытша. Табиғи инсулинді алмастырғышты, мысалы генетикалық жолмен алынған затты қолдану қант диабетін емдеуге керемет қосымша болып табылады. Бұл глюкозаның жасушаларға көбірек сіңіп, оны тасымалдау процестерінің өзгеруіне байланысты қант деңгейін төмендетуге көмектеседі. Бірақ бұл дәрі-дәрмектерді дәрігердің нұсқауы бойынша қатаң қолдану керек, өйткені олар пациенттің денсаулығына жағымсыз әсер етуі мүмкін. Инсулин 1 типті қант диабетін емдеудің негізгі дәрісі болып табылады. Кейде бұл аурудың екінші түріндегі науқасты тұрақтандыру және оның әл-ауқатын жақсарту үшін де қолданылады. Бұл зат табиғаты бойынша аз мөлшерде көмірсулар алмасуына әсер ететін гормон болып табылады. Әдетте, ұйқы безі инсулинді жеткілікті мөлшерде шығарады, бұл қандағы қанттың физиологиялық деңгейін ұстап тұруға көмектеседі. Бірақ ауыр эндокринді бұзылулармен науқасқа жиі көмектесудің жалғыз мүмкіндігі дәл инсулин инъекциясы болып табылады. Өкінішке орай, оны ауызша (таблетка түрінде) қабылдау мүмкін емес, өйткені ол ас қорыту жолында толығымен жойылып, биологиялық құндылығын жоғалтады. Бұл гормонды шошқалар мен ірі қара малдың ұйқы безінен алу - бүгінде сирек қолданылатын ескі технология. Бұл қабылданған дәрі-дәрмектердің сапасының төмендігімен, аллергиялық реакцияларға бейімділігімен және жеткіліксіз тазарту деңгейімен байланысты. Гормон ақуыздық зат болғандықтан, ол аминқышқылдарының белгілі бір жиынтығынан тұрады. Шошқаның денесінде өндірілетін инсулин аминқышқылдарының құрамы бойынша адам инсулинінен 1 амин қышқылына, ал мал азықтық инсулинге 3-тен ерекшеленеді. ХХ ғасырдың басында және ортасында, ұқсас препараттар болмаған кезде, тіпті мұндай инсулин медицинада жаңалық болды және қант диабетімен ауыратындарды емдеуді жаңа деңгейге көтеруге мүмкіндік берді. Осы әдіспен алынған гормондар қандағы қантты азайтты, алайда олар көбінесе жанама әсерлер мен аллергияны тудырды. Медицинадағы аминқышқылдары мен қоспалардың құрамындағы айырмашылық пациенттердің жағдайына әсер етті, әсіресе пациенттердің әлсіз топтарында (балалар мен қарттар). Мұндай инсулиннің нашар толеранттылығының тағы бір себебі - бұл препаратта оның белсенді емес прекурсорының болуы (проинсулин), бұл дәрі-дәрмектің өзгеруінен құтылу мүмкін болмады. Қазір бұл кемшіліктерден айырылған дамыған шошқа етінің инсулиндері бар. Олар шошқаның ұйқы безінен алынған, бірақ содан кейін олар қосымша өңдеуге және тазартуға ұшырайды. Олар көп компонентті және құрамында қосымша заттар бар. Шошқа етінің модификацияланған инсулині іс жүзінде адам гормонынан ерекшеленбейді, сондықтан ол практикада әлі де қолданылады Мұндай препараттарды пациенттер жақсырақ қабылдайды және іс жүзінде жағымсыз реакциялар туғызбайды, иммундық жүйені тежемейді және қандағы қантты тиімді төмендетеді. Ірі қара малының инсулині бүгінде медицинада қолданылмайды, өйткені оның сыртқы құрылымына байланысты ол иммундық және адам ағзасының басқа жүйелеріне теріс әсер етеді. Қант диабетімен ауыратындарға қолданылатын инсулинді өнеркәсіптік масштабта екі жолмен алады: Инсулинді сақтау шарттарыКөрсеткіштері және қарсы көрсетілімдері
Дәрілердің фармакологиялық әсері
Адамның генетикалық инженирленген дәрілерінің мысалдары
Инсулин неден жасалады?

Жануарлардан алынатын шикізаттан алынған препараттар
Генетикалық инженерлік инсулин
Физика-химиялық өзгеріске байланысты арнайы ферменттер әсерінен фарфор инсулинінің молекулалары адам инсулиніне ұқсас болады. Алынған препараттың амин қышқылының құрамы адам ағзасында өндірілетін табиғи гормонның құрамынан еш айырмашылығы жоқ.
Өндіріс барысында дәрі жоғары тазартудан өтеді, сондықтан аллергиялық реакциялар мен басқа да жағымсыз көріністер тудырмайды.
Бірақ инсулин көбінесе өзгертілген (генетикалық түрлендірілген) микроорганизмдердің көмегімен алынады. Биотехнологиялық әдістерді қолдана отырып, бактериялар немесе ашытқылар өздері инсулин шығара алатындай етіп өзгертіледі.
Инсулинді өндіруден басқа, оны тазарту маңызды рөл атқарады. Препарат аллергиялық және қабыну реакцияларын тудырмайтындай, әр кезеңде микроорганизмдер штамдарының және барлық ерітінділердің, сондай-ақ қолданылатын ингредиенттердің тазалығын бақылау қажет.
Мұндай инсулинді өндірудің 2 әдісі бар. Олардың біріншісі бір микроорганизмнің екі түрлі штамдарын (түрлерін) қолдануға негізделген.
Олардың әрқайсысы гормон ДНҚ молекуласының тек бір тізбегін синтездейді (олардың тек екеуі ғана бар және олар спиральды түрде бұралған).
Содан кейін бұл тізбектер қосылады, нәтижесінде алынған инсулиннің белсенді формаларын ешқандай биологиялық маңызы жоқтардан бөліп алуға болады.
Escherichia coli немесе ашытқыны қолданып дәрі-дәрмекті алудың екінші әдісі микробтың алдымен белсенді емес инсулинді (яғни, оның прединсулині) шығаратындығына негізделген. Содан кейін ферментативті емнің көмегімен бұл форма іске қосылып, медицинада қолданылады.
Белгілі бір өндіріс орындарына кіруге рұқсаты бар қызметкерлер әрдайым дәрінің адамның биологиялық сұйықтықтарымен байланысын болдырмайтын стерильді қорғаныс костюмімен киілуі керек.
Бұл процестердің барлығы әдетте автоматтандырылған, ауа және ампулалар мен шишалармен жанасатын барлық беттер зарарсыздандырылған, ал жабдықтары бар сызықтар герметикалық түрде жабылған.
Биотехнология әдістері ғалымдарға қант диабетінің балама шешімдері туралы ойлауға мүмкіндік береді.
Мәселен, қазіргі кезде генетикалық инженерия әдістерін қолдану арқылы жасанды панкреатиялық бета жасушаларын өндіруге клиникалық зерттеулер жүргізілуде.
Мүмкін болашақта олар ауру адамда осы ағзаның жұмысын жақсарту үшін қолданылуы мүмкін.
Қазіргі заманғы инсулин препараттарының өндірісі - бұл автоматтандыруды және адамның минималды араласуын қамтитын күрделі технологиялық процесс
Қосымша компоненттер
Қазіргі әлемде инсулиннің қоспасыз қосындысын елестету мүмкін емес, өйткені олар оның химиялық қасиеттерін жақсарта алады, әсер ету уақытын ұзартады және жоғары дәрежеде тазалыққа қол жеткізеді.
Қасиеттері бойынша барлық қосымша ингредиенттерді келесі сыныптарға бөлуге болады:
- пролонгаторлар (препараттың ұзақ әсер етуін қамтамасыз ету үшін қолданылатын заттар),
- дезинфекциялық компоненттер
- препарат ерітіндісінде оңтайлы қышқылдық сақталатын тұрақтандырғыштар.
Ұзартқыш қоспалар
Биологиялық белсенділігі 8-ден 42 сағатқа дейін созылатын ұзақ уақыт жұмыс істейтін инсулиндер бар (препараттың тобына байланысты). Бұл әсерге арнайы заттарды - пролонгаторларды инъекциялық ерітіндіге қосудың арқасында қол жеткізіледі. Бұл үшін көбінесе келесі қосылыстардың бірі қолданылады:
Препараттың әсерін ұзартатын ақуыздар толық тазартудан өтеді және аллергияға аз (мысалы, протамин). Мырыш тұздары инсулин белсенділігіне де, адамның әл-ауқатына да кері әсерін тигізбейді.
Инсулин құрамындағы дезинфекциялық заттар сақтау және қолдану кезінде микробтық флора көбейіп кетпеуі үшін қажет. Бұл заттар консерванттар болып табылады және препараттың биологиялық белсенділігінің сақталуын қамтамасыз етеді.
Сонымен қатар, егер пациент гормонды бір шишадан өзіне өзі басқарса, онда дәрі бірнеше күнге созылуы мүмкін.
Жоғары сапалы бактерияға қарсы компоненттердің арқасында ол микробтар ерітіндісінде көбеюдің теориялық мүмкіндігіне байланысты қолданылмаған дәріні тастаудың қажеті болмайды.
Инсулинді өндіруде келесі заттарды залалсыздандырғыш ретінде пайдалануға болады:
Егер ерітіндіде мырыш иондары болса, олар сонымен қатар микробқа қарсы қасиеттеріне байланысты қосымша консервант қызметін атқарады
Инсулиннің әр түрін шығару үшін белгілі бір дезинфекциялық компоненттер қолайлы. Олардың гормонмен өзара әрекеттесуі клиникаға дейінгі зерттеулер кезеңінде зерттелуі керек, өйткені консервант инсулиннің биологиялық белсенділігін бұзбауы немесе оның қасиеттеріне теріс әсер етпеуі керек.
Консерванттарды қолдану көп жағдайда гормонды алкогольмен немесе басқа антисептиктермен алдын-ала өңдеусіз тері астына енгізуге мүмкіндік береді (өндіруші бұл туралы нұсқаулықта жиі айтады).
Бұл препарат қабылдауды жеңілдетеді және инъекцияға дейін дайындық манипуляцияларының санын азайтады.
Бірақ бұл ұсыныс жеке инсулин шприцін жұқа инемен қолданған жағдайда ғана жұмыс істейді.
Тұрақтандырғыштар
Ерітіндінің рН берілген деңгейде сақталуы үшін тұрақтандырғыш қажет. Препараттың сақталуы, оның белсенділігі және химиялық қасиеттерінің тұрақтылығы қышқылдық деңгейіне байланысты. Қант диабетімен ауыратын науқастарға арналған инъекциялық гормонды өндіруде әдетте осы мақсатта фосфаттар қолданылады.
Мырышпен инсулин үшін ерітінді тұрақтандырғыштары әрдайым қажет емес, өйткені металл иондары қажетті тепе-теңдікті сақтауға көмектеседі.
Егер олар әлі де қолданылмаса, онда фосфаттардың орнына басқа химиялық қосылыстар қолданылады, өйткені бұл заттардың жиынтығы жауын-шашын мен препараттың жарамсыздығына әкеледі.
Барлық тұрақтандырғыштарға көрсетілген маңызды қасиет - бұл қауіпсіздік және инсулинмен кез-келген реакцияға түсе алмау.
Құзыретті эндокринолог әр науқас үшін қант диабеті үшін инъекциялық препараттарды таңдаумен айналысуы керек.
Инсулиннің міндеті - қандағы қанттың қалыпты деңгейін ұстап қана қоймай, сонымен қатар басқа мүшелер мен жүйелерге зиян тигізбеу. Препарат химиялық бейтарап, төмен аллергенді және жақсырақ қол жетімді болуы керек.
Егер таңдалған инсулинді әрекет ету мерзіміне сәйкес басқа нұсқаларымен араластыруға болатын болса, бұл өте ыңғайлы.
Инсулин алу, гендік инженерия әдістері, биотехнология - курстық жұмыс

1. Инсулиннің құрылымы мен функциялары 5
1.1. 5 инсулин молекуласының құрылымы
1.2. Инсулиннің биологиялық маңызы 7
1.3. Инсулин биосинтезі 8
2. Инсулиннің генетикалық инженериясы 10
2.1. Дәрілерді синтездеу үшін гендік инженерлік әдістерді қолдану 10
2.2. Генетикалық инженерия әдістері 11
2.3. Инсулиннің гендік инженериясы 14